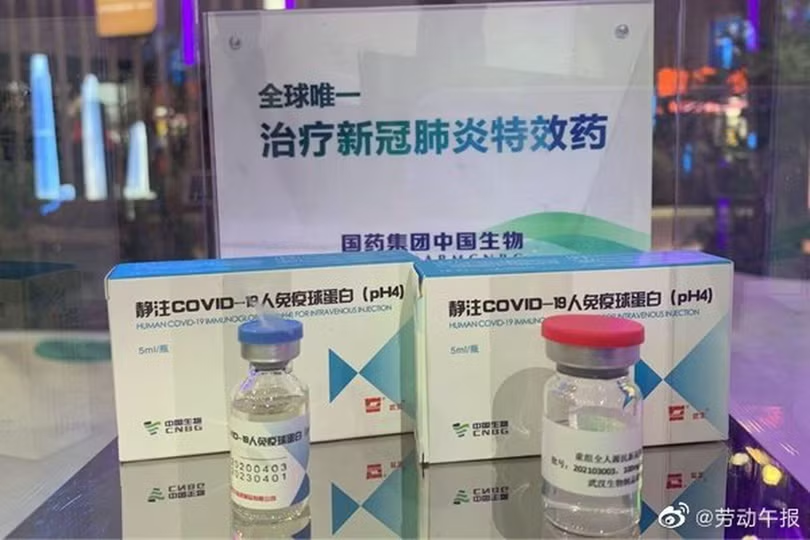
Theo truyền thông Trung Quốc Thời báo Hoàn cầu ngày 6/9, loại thuốc này có tên là "Human Immunoglobulin (pH4)" tiêm tĩnh mạch được Tập đoàn Công nghệ sinh học Sinopharm Trung Quốc phát triển, đã được Cục Quản lý Dược phẩm Quốc gia phê duyệt để thử nghiệm lâm sàng hôm 30/8.
Ông Trần Khôn (Chen Kun), Bí thư của Ủy ban Kiểm tra Kỷ luật Sinh học Trung Quốc, chỉ ra rằng immunoglobulin (globulin miễn dịch) ở người có tác dụng điều trị rất tốt đối với những người bị nhiễm virus biến thể Delta: “Những bệnh nhân nhiễm biến chủng Delta sử dụng thuốc này có tỷ lệ chữa khỏi là 100%”. Loại thuốc này gần đây đã được chính thức ra mắt hại Hội chợ dịch vụ thương mại quốc tế Trung Quốc (CIFTIS) năm 2021, diễn ra từ ngày 3 đến 7/9.
Mạng Tin tức Trung Quốc (China News Service) ngày 6/9 dẫn lời ông Trần Khôn cho biết, globulin miễn dịch được tạo ra từ huyết tương người khỏe mạnh đã được chủng ngừa bằng vaccine bất hoạt COVID-19 sinh học mới của Trung Quốc, chứa chất human immunoglobulin đặc hiệu tiêm tĩnh mạch kháng thể trung hòa SARS-CoV-2 hiệu quả cao. Ông tiết lộ rằng human immunoglobulin đã được áp dụng cho những người bị nhiễm bệnh và kết quả thử nghiệm rất tốt đối với loại virus biến thể Delta.
 |
| Khai mạc Hội chợ dịch vụ Thương mại Quốc tế Trung Quốc, ông Tập Cận Bình chúc mừng qua truyền hình (Ảnh: Xinhua). |
Trần Khôn cho biết: “Tỷ lệ chữa khỏi cho những bệnh nhân đã dùng thuốc này là 100% và không có trường hợp nào bị tử vong”. Ông giải thích rằng nguyên lý gây bệnh của virus không thay đổi và vẫn nằm trong phạm vi điều trị của thuốc, cho nên hiệu quả điều trị lâm sàng của loại thuốc đặc hiệu này đối với bệnh nhân không hề bị giảm khi virus bị biến đổi. Đối với việc khi nào loại thuốc cụ thể này sẽ được bán trên thị trường, Trần Khôn nói rằng tạm thời vẫn chưa xác định.
Vậy liệu thuốc đặc trị này liệu có thể được bán ra thị trường trong năm nay không? Trả lời phỏng vấn của phóng viên Thời báo Hoàn cầu ngày 5/9, ông Trần Khôn cho biết thời điểm đưa ra thị trường cụ thể không dễ xác định, bởi việc kiểm định thuốc của Trung Quốc rất nghiêm ngặt. Hơn nữa, theo thông lệ quốc tế, quá trình thử nghiệm lâm sàng một loại thuốc có thể kéo dài từ bảy đến tám năm. Nhưng chưa có tiền lệ về các loại thuốc đặc trị cho bệnh COVID-19, vì vậy rất khó để nói thử nghiệm lâm sàng sẽ kéo dài bao lâu. Tuy nhiên, ông nói rằng do hoàn cảnh đặc biệt của dịch bệnh, vaccine COVID-19 cũng đã phá vỡ thông lệ, từ khi nghiên cứu, thử nghiệm đến khi được đưa ra thị trường đều áp dụng chính sách đặc biệt, rút ngắn thời gian rất nhiều. Đối với phương án thử nghiệm lâm sàng cho thuốc đặc trị "chúng tôi đang hoạch định, nhưng sẽ rất nhanh".
Ông Trịnh Trung Vĩ (Zheng Zhongwei), Giám đốc Trung tâm Nghiên cứu Phát triển Công nghệ Y dược Y tế của Ủy ban Y tế và Sức khỏe Quốc gia Trung Quốc, phát biểu tại diễn đàn của Hội chợ Thương mại và Dịch vụ quốc tế rằng sự kết hợp “3 trong 1” giữa y tế công cộng, vaccine và thuốc điều trị là một chiến lược để chấm dứt dịch bệnh. Kiểm soát và phòng ngừa là việc cấp bách, vaccine là vũ khí cuối cùng để thắng dịch, còn thuốc là biện pháp quan trọng để dập dịch.
Tại Hội chợ Thương mại Dịch vụ Quốc tế Trung Quốc, Tập đoàn Công nghệ sinh học Trung Quốc Sinopharm cũng đã đưa ra bốn loại vaccine COVID-19 mới, bao gồm vaccine bất hoạt thế hệ thứ hai có thể vô hiệu hóa hiệu quả các chủng đột biến, vaccine di truyền tái tổ hợp gene và vaccine mRNA.
 |
| Ông Trần Khôn: Trung Quốc sẽ rút ngắn thời gian thử nghiệm lâm sàng đối với loại thuốc đặc trị COVID-19 (Ảnh: Creaders). |
Tập đoàn Sinopharm ngày 3/9 cho biết: “Thuốc globulin miễn dịch người (pH4) tiêm tĩnh mạch trị COVID-19 được Cục Quản lý Giám sát Dược phẩm Quốc gia phê duyệt và chấp thuận để thực hiện các thử nghiệm lâm sàng, có nghĩa là Trung Quốc đã trở thành quốc gia đầu tiên trên thế giới phát triển một loại thuốc đặc trị COVID-19 và Trung Quốc một lần nữa đứng hàng đầu thế giới trong cuộc chiến không có khói súng chống lại bệnh COVID-19!”. Sinopharm nói “đây lại là một thành tựu đột phá nữa của nhóm nghiên cứu trong lĩnh vực điều trị”.
Sinopharm nói thuốc đặc trị này được điều chế từ huyết tương người khỏe mạnh sau khi được tiêm chủng bằng vaccine bất hoạt coronavirus chủng mới của Trung Quốc đã được phê duyệt; sử dụng phương pháp tách và lọc protein bằng ethanol ở nhiệt độ thấp, cũng như các phương pháp khử hoạt tính và loại trừ để bào chế ra thuốc tiêm tĩnh mạch globulin miễn dịch người (pH4)
Thuốc này chủ yếu sử dụng điều trị chứng viêm phổi cấp do coronavirus chủng mới (COVID-19), được đóng gói với hai quy cách là 5000U/lọ (1,25g, 25ml) và 10.000U/lọ (2,5g, 50ml).
Sohu nói, trên thị trường thế giới không có sản phẩm cùng loại và cũng không có nhà sản xuất nào khác trên thế giới đăng kí thực hiện ứng dụng lâm sàng loại thuốc tiêm tĩnh mạch globulin miễn dịch người COVID-19 dựa trên huyết tương sau khi được chủng ngừa vaccine COVID-19. Trên thế giới hiện vẫn thiếu các phương pháp điều trị hoặc thuốc đặc hiệu cho bệnh COVID-19.