Cơ quan này cung cấp những lời khuyên khoa học và quy định cho các hãng sản xuất vaccine và đánh giá thông tin khoa học đối với mọi giai đoạn thử nghiệm lâm sàng – quy trình này còn tiếp tục ngay cả sau khi một chủng vaccine đã được FDA phê duyệt hoặc phê duyệt sử dụng khẩn cấp.
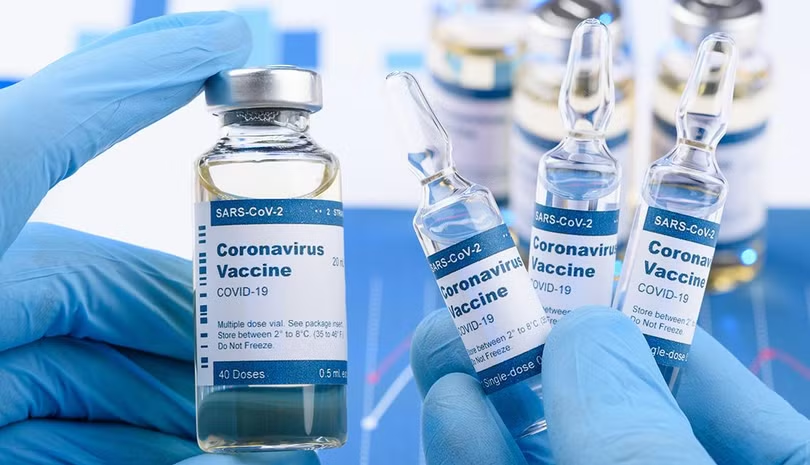
Đến nay, FDA đã phê duyệt 3 loại vaccine ngừa COVID-19 của Pfizer, Moderna và Johnson&Johnson, với hiệu quả và tính an toàn cao trong triển khai diện rộng.
Quy chế Sử dụng Khẩn cấp (EUA) là gì?
EUA là một cơ chế tạo điều kiện thuận lợi và sử dụng các biện pháp y tế, bao gồm cả vaccine, trong tình trạng khẩn cấp y tế công, như đại dịch COVID-19 hiện tại. Dưới cơ chế này, FDA có thể cho phép sử dụng các loại dược phẩm chưa được phê duyệt. Sauk hi xem xét các tiêu chí đầu vào của FDA, các hãng sản xuất sẽ quyết định về việc gửi đơn xin cấp phép EUA từ cơ quan này.
Một khi nhận được đơn yêu cầu, FDA sẽ đánh giá đề nghị EUA và quyết định xem các tiêu chí về pháp lý có được đáp ứng hay không, xem xét các bằng chứng khoa học về chủng vaccine sẵn có.
Vaccine COVID-19 được thử nghiệm như thế nào?
Các cuộc thử nghiệm lâm sàng vaccine COVID-19 đối với hàng chục nghìn người tham gia được thực hiện để thu về dữ liệu khoa học và những thông tin cần thiết mà FDA cần có để đánh giá về tính hiệu quả và an toàn của nó. Các cuộc thử nghiệm lâm sàng này được hiện theo tiêu chuẩn ngặt nghèo mà FDA đặt ra, chia làm 3 giai đoạn.
Giai đoạn 1: Vaccine được tiêm cho một nhóm nhỏ gồm những người khỏe mạnh để đánh giá độ an toàn khi tăng dần liều lượng và để thu được những thông tin sơ bộ về hiệu quả của vaccine trong việc sản sinh miễn dịch ở người. Nếu như không có vấn đề về an toàn trong thử nghiệm giai đoạn 1, giai đoạn 2 sẽ được bắt đầu.
Giai đoạn 2: Giai đoạn này được thực hiện với nhóm người lớn hơn, trong đó nhiều liều lượng khác nhau được thử nghiệm với hàng trăm người với tình trạng sức khỏe khác nhau và đến từ các nhóm tuổi khác nhau. Những nghiên cứu này cung cấp thêm thông tin về độ an toàn của vaccine, như các tác dụng phụ ngắn hạn cùng các rủi ro, tìm hiểu mối liên hệ giữa liều lượng sử dụng và phản ứng miễn dịch, và có thể cung cấp thông tin ban đầu về tính hiệu quả của vaccine.
Giai đoạn 3: Vaccine thường được thử nghiệm trên hàng nghìn người ở nhiều nhóm tuổi khác nhau (ví dụ như nhóm tuổi dự định được tiêm vaccine) và cung cấp thông tin quan trọng về tính hieuj quả cũng như mức độ an toàn của vaccine. Giai đoạn này cũng cung cấp thông tin thêm về phản ứng miễn dịch ở những người đã được tiêm vaccine so với những người được tiêm giả dược.
FDA cần những dữ liệu nào để có thể đánh giá cấp phép EUA?
Để một chủng vaccine nhận được EUA – nhằm đảm bảo chất lượng và tính nhất quán của sản phẩm – FDA cần đánh giá xem liệu lợi ích mà vaccine mang lại có vượt qua những nguy cơ tiềm ẩn của nó hay không.
Đề nghị EUA đối với một chủng vaccine COVID-19 có thể được gửi tới FDA dựa trên phân tích thử nghiệm tính hiệu quả của vaccine ở Giai đoạn 3 thử nghiệm lâm sàng hoặc phân tích nội bộ về giai đoạn thử nghiêm đó.
Trên phương diện độ an toàn, FDA yêu cầu một đơn xin EUA cần phải gửi kèm tất cả dữ liệu an toàn thu được từ Giai đoạn 1 và Giai đoạn 2 thử nghiệm vaccine. Cùng với đó là cơ sở dữ liệu an toàn trong Giai đoạn 3 thử nghiệm với hơn 3.000 người tham gia, tức đại diện cho một bộ phận lớn những người tham gia trong giai đoạn này – những người đã được theo dõi trong vòng ít nhất 1 tháng sau khi tiêm đầy đủ vaccine để xem có xuất hiện các phản ứng nghiêm trọng hay không.
Một phần trong quy trình đánh giá cấp phép EUA của FDA còn bao gồm đánh giá về thành phần hóa học, sản xuất và thông tin về vaccine. Mọi thông tin đầy đủ cần được gửi cho FDA để đảm bảo chất lượng và tính nhất quán của vaccine. FDA sẽ sử dụng tất cả công cụ và thông tin sẵn có để đánh giá xem quy trình sản xuất vaccine đã đạt tiêu chuẩn của họ hay chưa.
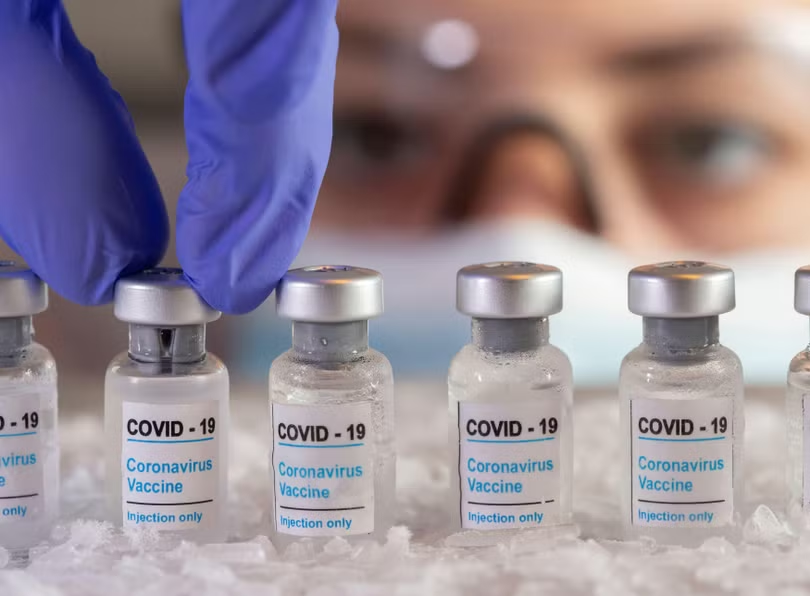 |
| Quy trình đánh giá của FDA đòi hỏi rất nhiều thông tin chi tiết về mức độ an toàn và hiệu quả của vaccine (Ảnh: CNBC) |
Quy trình đánh giá của FDA
Các hãng sản xuất vaccine sẽ phải thực hiện các cuộc thử nghiệm phi lâm sàng, lâm sàng với hàng chục nghìn người tham gia và sau đó gửi kết quả cho FDA. FDA sẽ đánh giá những thông tin này để đảm bảo độ an toàn và chất lượng của vaccine, đồng thời xem xem lợi ích mà vaccine đem lại có vượt qua rủi ro tiềm tàng của nó hay không.
Khi Giai đoạn 3 thử nghiệm lâm sàng trên người đạt đến điểm có thể đánh giá về khả năng chống COVID-19 của vaccine, một nhóm độc lập (gọi là ủy ban kiểm tra an dữ liệu an toàn) sẽ đánh giá thông tin và thông báo kết quả cho nhà sản xuất. Dựa trên dữ liệu và cách đánh giá dữ liệu của nhóm này, các nhà sản uất sẽ quyết định về thời điểm sẽ gửi đơn xin EUA tới FDA.
Sauk hi FDA nhận được đề nghị cấp EUA, các nhà khoa học của họ sẽ đánh giá tất cả thông tin liên quan mà nhà sản xuất gửi đến.
Trong lúc quy tình xem xét đang diễn ra, FDA sẽ tổ chức một cuộc họp công khai với Hội đồng Tư vấn Vaccine và Sinh phẩm liên quan (VRBPAC), bao gồm các chuyên gia khoa học và y tế đến từ khắp nước Mỹ. Trong cuộc họp này, các chuyên gia – đã được kiểm tra để loại bỏ khả năng xảy ra xung đột về lợi ích – sẽ thảo luận về dữ liệu an toàn và hiệu quả, công khai để cộng đồng khoa học và người dân hiểu rõ về dữ liệu mà FDA đang đánh giá, từ đó đưa ra quyết định xem có nên cấp EUA cho vaccine hay không.
Sau cuộc họp này, đội ngũ chuyên gia của FDA sẽ xem xét đầu vào của các thành viên trong hội đồng tư vấn, và tiếp tục đưa ra đánh giá riêng của họ về mức độ an toàn cũng như tính hiệu quả của vaccine.
Theo dõi vaccine COVID-19 sau khi đã được FDA phê duyệt sử dụng khẩn cấp
Các nhà sản xuất vaccine cũng cần phải gửi cho FDA kế hoạch theo dõi mức độ an toàn của vaccine sau khi đã nhận được EUA, bao gồm những trường hợp tử vong, tỷ lệ nhập viện, cùng nhiều phản ứng phụ nghiêm trọng khác…từ đó đưa ra cân nhắc về lợi ích/rủi ro, quyết định xem có nên tiếp tục duy trì EUA hay không.
FDA cũng yêu cầu các hãng sản xuất đã nhận được EUA tiếp tục thực hiện các cuộc thử nghiệm lâm sàng để có thêm thông tin về mức độ an toàn, tính hiệu quả của vaccine.
Việc kiểm soát độ an toàn của vaccine giai đoạn sau khi được phê chuẩn là trách nhiệm chung của FDA, Trung tâm Kiểm soát và Ngăn ngừa dịch bệnh (CDC) cùng các cơ quan hữu quan khác như Hệ thống báo cáo sự cố bất lợi của vaccine (VAERS), Vaccine Safety Datalink (VSD), Sáng kiến về Tác dụng và An Toàn Sinh học (BEST) và Medicare.
Theo FDA