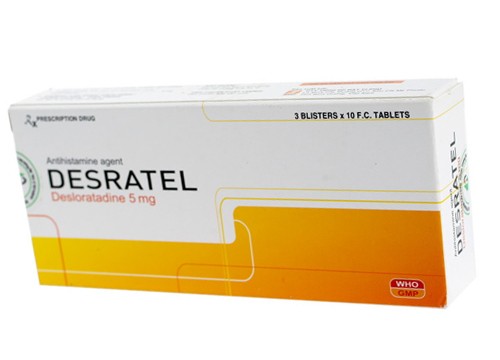
Theo đó, căn cứ vào quy chế dược hiện hành và công văn gửi kèm phiếu kiểm nghiệm của Viện Kiểm nghiệm thuốc TP. Hồ Chí Minh báo cáo lô thuốc viên nén bao phim Desteral (Desloratadin 5mg), SĐK: VD-28452-17, Số lô: 190157; HD: 19/2/2022 do Công ty cổ phần dược phẩm Đạt Vi Phú sản xuất và mẫu thuốc do Viện Kiểm nghiệm thuốc TP. Hồ Chí Minh lấy tại Công ty cổ phần dược phẩm Đạt Vi Phú, phát hiện thuốc không đạt tiêu chuẩn về chỉ tiêu định lượng (vi phạm mức độ 2).
Do đó, Cục Quản lý Dược yêu cầu thu hồi toàn quốc viên nén bao phim Desteral (Desloratadin 5mg) do Công ty cổ phần dược phẩm Đạt Vi Phú sản xuất.
 |
Trong thời hạn 48h kể từ ngày ký công văn, Cục Quản lý dược yêu cầu Công ty cổ phần dược phẩm Đạt Vi Phú cùng các nhà phân phối thuốc phải gửi thông báo thu hồi tới các cơ sở bán buôn, bán lẻ, sử dụng viên nén bao phim Desteral. Cùng với đó, gửi báo cáo thu hồi về Cục quản lý Dược trong vòng 18 ngày kể từ ngày ký công văn.
Cùng với thuốc Desratel (Desloratadin 5mg), Cục Quản lý Dược cũng yêu cầu đình chỉ lưu hành thuốc Cetirizin (Cetirizine 2HCL 10mg) do không đạt tiêu chuẩn chất lượng.
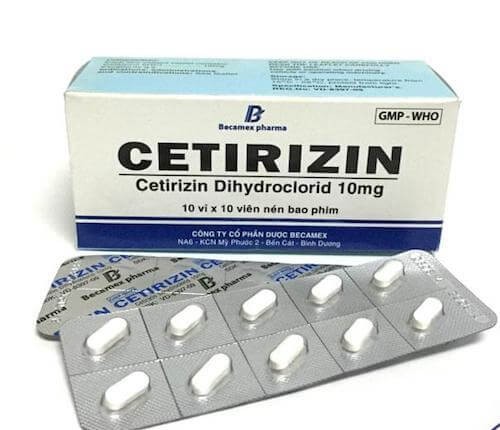 |
| Thuốc Cetirizin (Cetirizine 2HCL 10mg) |
Được biết, lô thuốc viên nén dài bao phim Cetirizin (Cetirizine 2HCL 10mg) do Công ty Cổ phần Dược phẩm 3/2 sản xuất không đạt tiêu chuẩn chất lượng về chỉ tiêu độ hòa tan (vi phạm mức độ 3).
 |
Cục Quản lý Dược đề nghị Sở Y tế các tỉnh, thành phố trực thuộc trung ương, Y tế các ngành thông báo cho các cơ sở kinh doanh, sử dụng thuốc thu hồi hai lô thuốc không đạt chất lượng nêu trên và kiểm tra, giám sát các đơn vị thực hiện thông báo; xử lý những đơn vị vi phạm theo quy định hiện hành, báo cáo về Cục Quản lý Dược và các cơ quan chức năng có liên quan.








































Bình luận của bạn đọc
Bình luận bằng tài khoản VietTimes
Bình luận bằng tài khoản mạng xã hội
Xin vui lòng gõ tiếng Việt có dấu